Artículos de interés
![]()
CONSIDERACIONES EN LA ESTIMACIÓN DE LA EXPOSICIÓN HUMANA AL ARSÉNICO
José Antonio Huamaní-Azorza1,a, Aurora Olegaria Huamolle-Barreto1,a, Carlos Huamaní-Pacsi 1,b, Guillermo Fernando Villa-Gonzales1,b
Resumen
En Perú, la presencia de arsénico (As) en agua para consumo humano proviene tanto de fuentes naturales como producto de las actividades humanas en minería, refinación de metales. Debido a su naturaleza como agente cancerígeno, es actualmente motivo de gran preocupación. Su toxicidad depende de la forma química; así, su presencia como arsenito es más tóxica que arsenato y ambas más que sus compuestos orgánicos. El arsénico total en orina es el biomarcador utilizado para estimar niveles de exposición. Sin embargo, en ocasiones esta forma de evaluación puede no ser la adecuada, pues la ingesta de alimentos en especial pescados y mariscos pueden elevar la concentración de arsénico urinario.
Palabras clave: arsénico, metabolismo, biomarcadores.
Introducción
En el medio ambiente, el arsénico (As) está presente en cuatro estados de oxidación diferentes (As-3, As0, As+3, As+5) en formas orgánicas e inorgánicas 1. La toxicidad y carcinogenicidad del arsénico está fuertemente asociada con sus estados de oxidación y formas químicas 2-4. Desde el punto de vista de la salud pública, el agua para consumo humano es la principal fuente de exposición al arsénico inorgánico; y su presencia en agua pone en riesgo a millones de personas que consumen este recurso con concentraciones por encima de 10 μg As/L 5.
En el agua superficial y subterránea, el arsénico se encuentra en estado de oxidación como arsenato (As+5) y arsenito (As+3). En aguas superficiales con alto contenido de oxígeno, la especie más común es el arsenato. Bajo condiciones de reducción, generalmente en los sedimentos de los lagos o aguas subterráneas, predomina la forma de arsenito. Los arsenatos y arsenitos se disocian a un pH muy diferente.
El pH es uno de los factores que controlan la especiación, y la movilidad del elemento en los distintos cuerpos de agua (subterráneas, lagos, mar, aguas profundas, ríos, etc.) 6.
El proceso de penetración del arsénico desde el ambiente hasta su órgano diana, donde producirá su efecto tóxico, puede dividirse en tres etapas:
1. Etapa de exposición, considera procesos de interacción entre diversos tóxicos y/o la influencia de los factores ambientales sobre los mismos.
2. Etapa toxicocinética, que comprende la absorción, distribución y acumulación en tejidos y/o órganos, biotransformación o metabolismo y eliminación o excreción de formas metabolizadas y no metabolizadas.
3. Etapa toxicodinámica, que se refiere a cómo los xenobióticos o sus metabolitos ejercen sus efectos a través de interacciones moleculares con lugares de acción específicos en las células, con el resultado de un efecto toxico 7.
Exposición
La exposición prolongada al arsénico, a través del consumo de agua, alimentos a base de pescados, mariscos o cultivos alimentarios regados con agua contaminada, representan un riesgo latente de intoxicación crónica.
Metabolismo
El cuerpo humano tiene la capacidad de transformar arsénico de forma inorgánica a orgánica mediante reacciones de metilación, lo que facilita su eliminación. Para que se lleve a cabo este fenómeno de biotransformación, el arsenato (As+5) sufre dos fases: la Fase I determinada por reacciones de oxidación / reducción que interconectan las reacciones de arsenito/arsenato y una Fase II en la que hay reacciones de conjugación, catalizada por metiltransferasas, que convierten el arsenito en formas metiladas, como ácido monometilarsónico (MMA) y ácido dimetilarsínico (DMA). La serie de reacciones da como resultado la reducción de arsenato inorgánico a arsenito, metilación a MMA (V), reducción a MMA (III) y metilación a DMA (V) 8, tal como muestra la Figura 1.
Según la Agencia para Sustancias Toxicas y el Registro de Enfermedades (ATSDR, por sus siglas en inglés) de los EE. UU, se estima que la población presenta proporciones aproximadas de DMA en 40 a 75%, arsénico inorgánico de 20 a 25% y MMA 8 de 15 a 25%. Sin embargo, factores como la concentración de arsénico en el agua, etnia, dieta, sexo o edad podrían afectar los niveles individuales de arsénico metilado en orina 9.
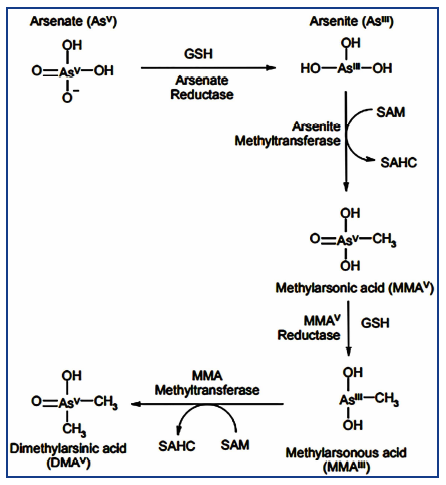
Figura 1: Biotransformación de arsénico inorgánico
Fuente: ATSDR; 2007. Disponible en: https://www.atsdr.cdc.gov/toxprofiles/tp2.pdf
El consumo de alimentos, principalmente peces y mariscos, representan otra fuente de exposición, pues aportan formas orgánicas de arsénico como la arsenobetaína y arsenocolina (Figura 2). Su vida media aproximada es de 4 horas y se excretan completamente por orina entre 1 y 2 días sin formar metabolitos residuales, llegando a considerarse como productos de baja toxicidad. 8,10-12.
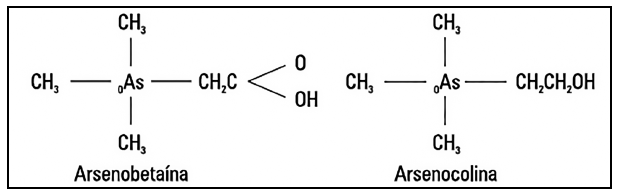
Figura 2. Arsenobetaína y arsenocolina
Fuente: Ramirez AV; 2013. Disponible en: http://www.scielo.org.pe/scielo.php?script=sci_arttext&pid=S1025-55832013000300014
Biomarcador de exposición
Los biomarcadores de exposición son generalmente el mismo xenobiótico, o sus metabolitos específicos presente en fluidos corporales como productos de reacciones bioquímicas que se dan a nivel del organismo.
Los efectos tóxicos a largo plazo del arsénico se deben principalmente a la exposición de sus formas inorgánicas, siendo la cuantificación de arsénico total en orina un parámetro para estimar su exposición13. Sin embargo, ésta forma de cuantificación no discrimina las especies de alta y baja toxicidad, por lo que podría no ser la mejor forma de evaluación toxicológica.
Estimación de la exposición
McClintock et.al. (2012) 1 menciona que los alimentos son otra fuente de arsénico en países latinoamericanos y algunos estudios de áreas endémicas han indicado que los alimentos aportan hasta el 50% de la ingesta total de arsénico.
De acuerdo a la evidencia científica una limitación del uso del arsénico urinario total como biomarcador de exposición es que la arsenobetaína y arsenocolina son excretados en la orina después de la ingesta de ciertos alimentos como peces y mariscos. Los métodos analíticos basados en la cuantificación de arsénico total en orina pueden sobreestimar la exposición real de las especies inorgánicas y metiladas de interés toxicológico.
Debido a esta interferencia la Guía de Práctica Clínica para el Diagnóstico y Tratamiento de la Intoxicación por arsénico aprobado mediante RM N°389-2011/MINSA 13 recomienda evitar el consumo de peces, mariscos y moluscos por lo menos 48 horas antes de realizarse el examen de arsénico en orina.
En casos donde la concentración de arsénico total en orina sea elevada y se sospeche consumo de alimentos marinos, la ATSDR recomienda realizar la cuantificación de una o más especies químicas en una muestra mediante un análisis de especiación 14 a fin de cuantificar las especies de interés toxicológico, tales como arsénico inorgánico y sus formas metiladas (MMA y DMA)15.
Conclusiones
Las especies inorgánicas de arsénico presentes en el agua de consumo humano representan un riesgo a la salud. Los seres humanos metabolizan el arsénico ingerido a través de reacciones bioquímicas de oxido/reducción (Fase I) y conjugación (Fase II), seguido de excreción urinaria.
El arsénico total en orina es el biomarcador utilizado para determinar niveles de exposición. Sin embargo, en ocasiones esta forma de evaluación puede no ser la adecuada; pues la ingesta de alimentos (pescados y mariscos, principalmente) pueden elevar la concentración de arsénico urinario debido al aporte de especies de baja toxicidad como la arsenobetaína y arsenocolina..
Referencias Bibliográficas
1. McClintock TR, Chen Y, Bundschuh J, Oliver JT, Navoni J, Olmos V, et al. Arsenic exposure in Latin America: biomarkers, risk assessments and related health effects. Sci Total Environ. 2012;429:76–91. doi: 10.1016/j.scitotenv.2011.08.051
2. International Agency for Research on Cancer. Some drinking-water disinfectants and contaminants, including arsenic. [Internet] IARC Monogr Eval Carcinog Risks Hum. 2004; 84: 1-477. Disponible en: https://www.ncbi.nlm.nih.gov/books/NBK402251/pdf/Bookshelf_NBK402251.pdf
3. Kuo, CC, Moon, KA, Wang, SL, Silbergeld, E, Navas-Acien, A. The Association of Arsenic Metabolism with Cancer, Cardiovascular Disease, and Diabetes: A Systematic Review of the Epidemiological Evidence. Environ Health Perspect. 2017;125(8):087001. doi: 10.1289/EHP577
4. Lorenc W, Kruszka D, Kachlicki P, Kozłowska J, Barałkiewicz D. (2020). Arsenic species and their transformation pathways in marine plants. Usefulness of advanced hyphenated techniques HPLC/ICP-MS and UPLC/ESI-MS/MS in arsenic species analysis. Talanta. 2020;220. doi:10.1016/j.talanta.2020.121384
5. Arsenic in Drinking-water [Internet]. World Health Organization. 2003 [consultado 13 julio 2020]. Disponible en: https://apps.who.int/iris/bitstream/handle/10665/75375/WHO_SDE_WSH_03.04_75_eng.pdf;jsessionid=E33D07196EB82042E4F14F2A9E6D89DB?sequence=1
6. Litter M, Armienta M, Farias S. IBEROARSEN: metodologías analíticas para la determinación y especiación de arsénico en aguas y suelos. [Internet] Buenos Aires: CYTED; 2009, 242 p. Disponible en: https://paginas.fe.up.pt/~cigar/html/documents/Monografia2_000.pdf
7. Repetto-Jiménez M, Repetto Kuhn G. Toxicología fundamental. [Internet]. 4a ed. España: Díaz de Santos; 2009. 35 p. Disponible en: https://www.editdiazdesantos.com/wwwdat/pdf/9788479788988.pdf
8. Agency for Toxic Substances and Disease Registry. Toxicological profile for arsenic. [Internet]. US Department of Health and Human Services, Public Health Service, Agency for Toxic Substances and Disease Registry: Atlanta, Georgia; 2007 [Consultado 08 Agosto 2017]. 559 p. Disponible en: https://www.atsdr.cdc.gov/toxprofiles/tp2.pdf.
9. Songbo F, Jie W, Yuanyuan L, Yan L, Yanhui G, Feifei Y, Chuanying Q, Li S, Yu W, Yongjian Li, Dianjun S. Urinary arsenic metabolism in a Western Chinese population exposed to high-dose inorganic arsenic in drinking water: Influence of ethnicity and genetic polymorphisms. Toxicol. Appl. Pharmacol. 2014; 274 (1): 117-23. doi: 10.1016/j.taap.2013.11.004
10. Ramirez AV. Exposición ocupacional y ambiental al arsénico. Actualización bibliográfica para investigación científica. An Fac med. 2013; 74(3):237-47. doi: 10.15381/anales.v74i3.2642
11. Medina-Pizzali M, Robles P, Mendoza M, Torres C. Ingesta de arsénico: el impacto en la alimentación y la salud humana. Rev Peru Med Exp Salud Publica. [Internet] 2018;35(1):93-102. Disponible en: https://rpmesp.ins.gob.pe/index.php/rpmesp/article/view/3604/2959
12. Navas-Acien A, Francesconi KA, Silbergeld EK, Guallar E. Seafood intake and urine concentrations of total arsenic, dimethylarsinate and arsenobetaine in the US population. Environ. res. 2011;111(1), 110-18. doi: 10.1016/j.envres.2010.10.009
13. Ministerio de Salud. Guía técnica: guía de práctica clínica para el diagnóstico y tratamiento de la intoxicación por arsénico. R.M. Nº 389-2011/ MINSA [Internet]. Lima: MINSA; 2011. 32 p. Disponible en: http://bvs.minsa.gob.pe/local/minsa/2109.pdf
14. Estudios de caso en medicina ambiental [Internet]. Agencia para Sustancias Toxicas y el Registro de Enfermedades. 2016 [consultado 15 julio 2020]. Disponible en: https://www.atsdr.cdc.gov/es/csem/arsenic/evaluacion_clinica.html
15. Gardner R, Hamadani J, Grandér M, Tofail F, Nermell B, Palm B, Kippler M, Vahter M. Persistent exposure to arsenic via drinking water in rural Bangladesh despite major mitigation efforts. Am. J. Public Health. 2011;101(S1) S333-8. doi: 10.2105/AJPH.2010.300025.










