CAPACIDAD DE RESPUESTA DEL LABORATORIO DE REFERENCIA NACIONAL DE VIRUS RESPIRATORIO PARA EL DIAGNÓSTICO MOLECULAR DEL SARS-COV-2 DURANTE LA PRIMERA OLA DE LA PANDEMIA DE LA COVID-19
Casquero-Cavero José1, Rojas-Serrano Nancy1, Huaringa-Núñez Maribel1, Salinas- Coronel Gabriela1, Portilla-Romero Janett1, Arotinco-Garayar Gloria1, Calvay-Sánchez Karen1, Villar-Saavedra Sandra1, Cabrera-Campos Bryan1, Pari-Lope Priscila1, Galindo- Sánchez Shana1, Munayco-Hernández Aldo1, Ramírez-Mori Juan1, Huamán-Angeles Estela1, Obregón-Boltan George1
Resumen
La capacidad de los laboratorios para detectar el SARS-CoV-2 ha sido clave para la contención de la enfermedad por coronavirus 2019 (COVID-19). El 15 de marzo de 2020, se declaró en el Perú el estado de emergencia nacional, contando el Instituto Nacional de Salud (INS) con la capacidad para realizar el diagnóstico molecular de 41 pruebas diarias. En 10 meses, el INS incrementó su capacidad a 6,000 pruebas diarias, procesando 575,493 muestras equivalentes al 36.2% de las pruebas a nivel nacional durante la primera ola pandémica.
Palabra clave: COVID–19, Instituto Nacional de Salud, Perú.
Introducción
El primer caso importado de la enfermedad por coronavirus 2019 (COVID-19) fue confirmado el 6 de marzo por el Laboratorio de Referencia Nacional de Virus Respiratorio del Instituto Nacional de Salud (LRNVRINS) mediante diagnóstico molecular1. El 15 de marzo el gobierno peruano declaró el estado de emergencia nacional a consecuencia de la COVID-192, indicándose que las muestras sean remitidas a los laboratorios de Referencia Regional y de éstos al INS3. Un estudio señaló que era “altamente probable que el número de personas contagiadas y fallecidas a causa de la COVID-19 siga aumentando en los próximos días y semanas”4. Al 31 de mayo, se registraron 155,671 casos, 4371 fallecidos con tendencia ascendente; por lo que se decidió ampliar la capacidad de respuesta del LRNVR-INS para atender la potencial demanda de la prueba molecular. El objetivo del estudio es describir el proceso de mejora de la capacidad del LRNVR-INS para el diagnóstico molecular del SARS-CoV-2 durante la primera ola de la pandemia de la COVID-19.
Material y Métodos
El análisis retrospectivo del incremento de la capacidad diagnóstica del LRNVR-INS fue sistematizado en tres fases, teniendo como criterios de evaluación las tecnologías de diagnóstico, personal, infraestructura y producción de pruebas moleculares.
Primera fase: Comenzó el 31 de enero de 2020 con el “Plan de acción ante el riesgo de introducción del nuevo Coronavirus” del INS y concluyó el 15 de marzo con la Declaración del Estado de Emergencia Nacional2. El diagnóstico molecular fue realizado íntegramente en el LRNVR-INS.
Segunda fase: Inició el 16 de marzo con el estado de emergencia nacional y aislamiento social obligatorio y terminó el 16 de junio al inaugurar el nuevo laboratorio de diagnóstico molecular para la detección de SARSCoV-2(COVID-19). La respuesta ante la demanda de las pruebas de Reacción en Cadena de la Polimerasa por Transcriptasa Reversa (RT-PCR) en tiempo real fue realizada por diversos laboratorios del INS.
Tercera fase: Empezó el 17 de junio y finalizó el 11 de enero de 2021, cuando se declaró la segunda ola de la pandemia5. Las pruebas moleculares fueron realizadas en el nuevo Laboratorio COVID-19.
Resultados
El estudio abarcó del 31 de enero 2020 al 11 de enero 2021, con 3 fases de desarrollo continuas y en escalamiento.
Primera fase
Comprendió desde la semana epidemiológica 6 a la 11. En febrero de 2020, se capacitó en Brasil personal del LRNVR-INS en el diagnóstico molecular del SARS-CoV-2 para implementar la RT-PCR en tiempo real manual. Las actividades pre-analíticas, diagnóstico molecular y post-analíticas fueron realizadas por 21 personas en jornadas de 24 horas durante 7 días divididos en grupos de trabajo. El área utilizada fue 93.44 m2. Se procesaron 1,725 hisopados nasales y faríngeos con un promedio de 41 pruebas diarias (gráfica 1).
Para registrar las solicitudes de diagnóstico, se desarrolló el módulo SARS-CoV-2 en el sistema de información de laboratorio NETLAB.v.2.0 centralizado en el INS para liberar los resultados en tiempo real, siendo la base de datos derivada al Centro Nacional de Epidemiología, Prevención y Control de Enfermedades para analizar y tomar decisiones en salud pública.
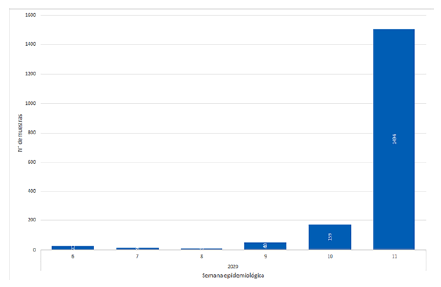
Grafica 1 . Número de muestras procesadas semanalmente en la primera fase6
Segunda fase
Abarcó desde la semana epidemiológica 12 a la 25. A la metodología de la fase inicial, se incorporaron el sistema cerrado de extracción y amplificación COBAS® 6800 (Roche), GeneXpert® (Cepheid), plataformas de extracción QIAsymphony (Qiagen), QIAcube Connect (Qiagen) y shock térmico para el RT-PCR Multiplex en tiempo real manual. La selección técnica priorizó el equipamiento instalado en los laboratorios, insumos y reactivos disponibles localmente. Existieron demoras en los abastecimientos de reactivos por restricciones internacionales.
Participaron 110 personas de diversos laboratorios del INS que también brindaron sus instalaciones, equipos, reactivos y consumibles. El personal participó en 2 turnos cubriendo las 24 horas los 7 días de la semana. Se añadieron 450.61 m2 a la superficie indicada en la primera fase.
Se procesaron 133,138 hisopados nasales y faríngeos (gráfica 2) y se aprobó el “Plan de implementación del laboratorio de diagnóstico molecular para la detección de SARS-CoV-2 (COVID-19)”7.
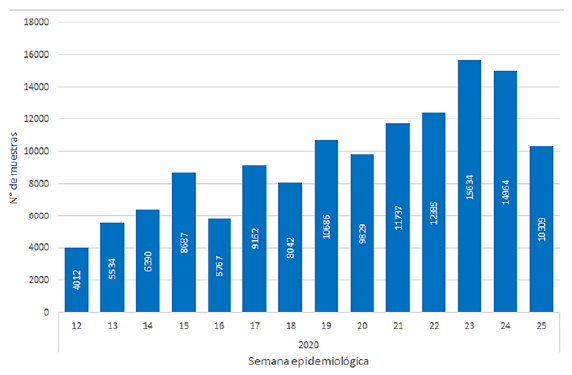
Gráfica 2. Número de muestras procesadas semanalmente en la segunda fase6
Tercera fase
Se extendió desde la semana epidemiológica 26 a la 53 de 2020 y primera de 2021. Se incrementó la capacidad de respuesta con el nuevo Laboratorio COVID-19 en un área de 307.3 m2. Se mejoró la infraestructura, sistema eléctrico, red de comunicación, e incorporó cámaras de video vigilancia, control de acceso facial con medición de temperatura, manejo de residuos (comunes, biocontaminados, especiales), NETLAB.v.2.0 y mobiliario.
Las plataformas de diagnóstico utilizadas fueron el sistema automatizado de extracción y amplificación MGISP-960 (MGI Tech Co., Ltd.) con termocicladores Bio-Rad y Sansure, Zybio EXM6000 (Zybio) con termocicladores Molarray y sistema de extracción Oktopure (LGC biosearch) con termocicladores Sansure y Bio-Rad.
Se adquirieron reactivos, consumibles, y equipos de laboratorio como autoclaves (MMM), cabinas de bioseguridad de clase II tipo A2 (Labconco) certificadas, cabinas de PCR (Cleaver Scientific), conservadoras de 2 a 8ºC (Medical Systems y Helmer), congeladoras de -20ºC,-40ºC y -80ºC (Thermo Fisher Scientific), micro centrífugas refrigeradas (Thermo Fisher Scientific), mini centrífugas refrigeradas (Biosan y Bio-Rad).
Se contrató a 96 personas para actividades pre-analíticas, diagnóstico molecular, post-analíticas y gestión administrativa. Esto permitió contar con una capacidad instalada para procesar entre 4000 a 6000 muestras diarias, lográndose procesar 440,630 muestras durante esta fase (gráfica 3).
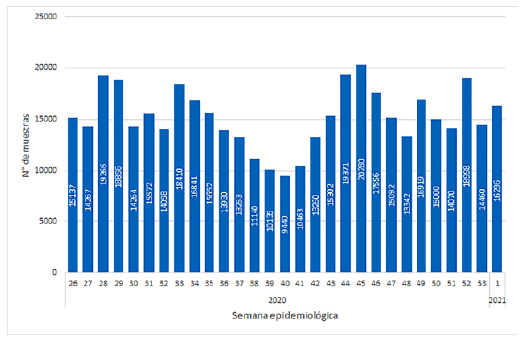
Gráfica 3. Número de muestras procesadas semanalmente en la tercera fase6
El INS realizó el 36.2% de las pruebas a nivel nacional durante la primera ola.
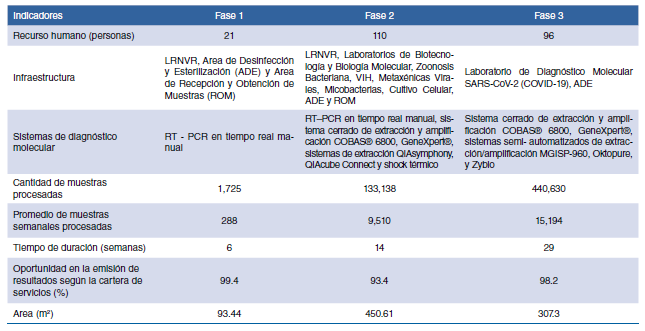
Instituciones internacionales y nacionales donaron insumos y equipos, contribuyendo al sostenimiento del diagnóstico, debido a las restricciones internacionales que desaceleraron la importación limitando la capacidad diagnóstica. La tabla 1, resume la distribución de las áreas, recurso humano, producción de pruebas por fase y entrega de resultados que osciló entre 3 a 5 días, cumpliendo en promedio con la meta de oportunidad en un 98.2%.
Se reforzaron las capacidades del personal mediante entrenamientos en las diversas plataformas moleculares, medidas de bioseguridad, gestión de la calidad basada en la ISO 15189, manejo de extintores, residuos y NETLAB.v.2.0. Se enfrentaron importantes desafíos, como el débil sistema de adquisiciones de materiales y la carente descentralización del ingreso de información en el NETLAB.v.2.0 desde el nivel periférico. En 2020, el LRNVR-INS participó en los programas de Evaluación Externa de la Calidad para la Detección de SARS-CoV-2 por RT-PCR de la Organización Mundial de la Salud (OMS) y del College of American Pathologists (CAP) SARS-CoV-2 evento B 2020, obteniendo concordancias de resultados del 100%.
Tabla 1. Distribución de áreas, recursos y producción por fases para el diagnóstico molecular en las instalaciones del INS durante la primera ola pandémica de la COVID-19
Discusión
La presencia de agentes infecciosos afectan la salud pública global. Sin embargo, las experiencias adquiridas por la aparición del SARS ocasionó la construcción de mejoras en la capacidad de respuesta de los laboratorios de referencia en bioseguridad, biocustodia, evaluaciones externas de la calidad, estandarización e implementación del diagnóstico molecular para responder con resultados rápidos, confiables y de calidad ante situaciones de vigilancia, brotes e investigación; estas mejoras en los laboratorios de países de bajos y medianos ingresos fueron escalonadas o en fases y en colaboración entre los gobiernos y la cooperación internacional, considerando infraestructura, capacitación del personal, equipamiento, insumos, estandarización de protocolos8-10, siendo similar a nuestra experiencia a lo largo de las 3 fases descritas. El INS realizó una de cada tres pruebas moleculares realizadas durante la primera ola pandémica a nivel nacional. El estudio
tuvo la dificultad en diferenciar el costo de los materiales de laboratorio debido a que las adquisiciones fueron realizadas conjuntamente para el INS y regiones hacia las cuales se descentralizó el diagnóstico molecular.
Agradecimiento
A todo el personal que participó en los diferentes procesos del diagnóstico molecular.
Referencias Bibliográficas
1. Instituto Nacional de Salud [Internet]. Lima: Instituto Nacional de Salud: [actualizado 17 de agosto de 2021]. Laboratorios que realizan pruebas moleculares para el diagnóstico de SARS CoV-2 (COVID-19); [11 de marzo de 2021]. Disponible en: https://web.ins.gob.pe/es/prensa/noticia/laboratorios-que-realizanpruebas-moleculares-para-el-diagnostico-de-sars-cov-2
2. Decreto Supremo que declara Estado de Emergencia Nacional por las graves circunstancias que afectan la vida de la Nación a consecuencia del brote del COVID-19. Decreto Supremo Nº 044-2020-PCM de 23 de marzo de 2020 [Internet]. Lima: Diario Oficial El Peruano, no. 1864948. Disponible en: https://busquedas.elperuano.pe/normaslegales/decreto-supremo-que-declara-estado-de-emergencia-nacional-po-decretosupremo-n-044-2020-pcm-1864948-2/
3. Centro Nacional de Epidemiologia, Prevención y Control de Enfermedades. Alerta Epidemiológica código: AE-014-2020 Alerta epidemiológica ante la evolución de la pandemia de COVID-19 en el Perú. [Internet]. Lima: Centro Nacional de Epidemiologia, Prevención y Control de Enfermedades; 2020. 12 p. Disponible en: https://www.gob.pe/institucion/minsa/informes-publicaciones/1126503-alerta-epidemiologica-ante-laevolucion-de-la-pandemia-de-covid-19-en-el-peru-alerta-epidemiologica-n-14
4. Gobierno y Políticas Públicas PUCP [Internet]. Lima: PUCP, Escuela de Gobierno y Políticas Públicas; [25 de noviembre de 2010]. Aragón J, Cruz M. Datos y tendencias del avance de COVID–19 en Perú después de 50 días del primer caso reportado y de 40 días de cuarentena: [29 de abril de 2020]; [aproximadamente 6 pantallas]. Disponible en: https://escuela.pucp.edu.pe/gobierno/investigacion/reportes-tematicos-2/datos-y-tendencias-del-avance-del-covid-19-en-peru/
5. SWI swissinfo.ch [Internet]. Berna, Suiza: Sociedad Suiza de Radiotelevisión (SRG SSR); [actualizado 4 de agosto de 2021]. Perú está inmerso en la segunda ola de covid-19, confirma ministra de Salud; [13 de enero de 2021]; [aproximadamente 2 pantallas]. Disponible en: <https://www.swissinfo.ch/spa/coronavirusperú_perú-está-inmerso-en-la-segunda-ola-de-covid-19–confirma-ministra-de-salud/46281798> [Acceso 16 Marzo 2021].
6. Instituto Nacional de Salud [Internet]. Lima: Instituto Nacional de Salud; [actualizado 17 de agosto de 2021]. Pruebas moleculares realizadas para el diagnóstico de COVID-19 [actualizado 22 de agosto de 2020]; [1 pantalla] Disponible en: https://web.ins.gob.pe/es/indicador/pruebas-moleculares-realizadas-para-eldiagnostico-de-covid-19
7. Resolución Directoral Nº 65-2020-DG-CNSP/INS que aprueba el “Plan de implementación del laboratorio de diagnóstico molecular para la detección de SARS-CoV-2 (COVID-19)”.
8. Hunsperger E, Juma B, Onyango C, Ochieng JB, Omballa V, y otros. Building laboratory capacity to detect and characterize pathogens of public and global health security concern in Kenya. BMC Public Health [Internet]. 2019;19(Suppl 3):477. DOI: https://doi.org/10.1186/s12889-019-6770-9
9. Paglia MG, Bevilacqua N, Haji HS, Vairo F, Girardi E y otros. Improvement of Tuberculosis Laboratory Capacity on Pemba Island, Zanzibar: A Health Cooperation Project. PLOS ONE. [Internet]. 2012;7(8):e44109. DOI: https://doi.org/10.1371/journal.pone.0044109
10. Drews SJ, Majury A, Jamieson F, Riley G, Mazzulli T, Low DE. A Decentralized Molecular Diagnostic Testing Plan for Pandemic Influenza in the Ontario Public Health Laboratory System. Can J Public Health. [Internet]. 2008;99(5):387-90. DOI: https://link.springer.com/article/10.1007%2FBF03405247
1 Centro Nacional de Salud Pública – Instituto Nacional de Salud
Citar como: Casquero-Cavero J, Rojas-Serrano N, Huaringa-Núñez M, Salinas-Coronel G, Portilla-Romero J, Arotinco-Garayar G, et al. Capacidad de Respuesta del Laboratorio de Referencia Nacional de Virus Respiratorio para el Diagnóstico Molecular del SARS – CoV – 2 durante la primera ola de la pandemia de la COVID – 19. Bol Inst. Nac. Salud. 2021;27 (9-10):114-119.










