ACREDITACIÓN DE LOS LABORATORIOS CLÍNICOS EN LATINOAMÉRICA
Fernando Alva Ruiz1
Resumen
Todo laboratorio clínico, de ensayo o calibración implementa un sistema de gestión de la calidad con el fin de asegurar que sus resultados sean válidos y confiables. Los laboratorios clínicos se acreditan con la ISO 15189 mientras que los demás laboratorios como el de ensayo y calibración se acreditan con la ISO/IEC 17025. Cada país cuenta con un organismo de acreditación que debe ser reconocido internacionalmente por el Foro Internacional de Acreditación (IAF), la Cooperación Internacional de Acreditación de Laboratorios (ILAC) y los organismos regionales de reconocimiento mutuo como la Cooperación Interamericana de Acreditación (IAAC). Estos organismos de acreditación de cada país deben cumplir la ISO/IEC 17011.
Una preocupante realidad en Latinoamérica, el porcentaje de laboratorios clínicos acreditados es notablemente bajo. Es una situación de inquietud ya que se requiere resultados precisos y confiables para el manejo de los pacientes. Para abordar este desafío, se requiere implementar estrategias a corto, mediano y largo plazo; las que deben estar diseñadas para impulsar un aumento significativo en el número de laboratorios acreditados, promoviendo así un estándar más elevado en calidad y confiabilidad en los servicios de diagnóstico de salud.
Palabras claves: Acreditación, laboratorios clínicos, ISO.
Introducción
La mejor opción para el sistema de gestión de un laboratorio clínico es implementar la norma ISO 15189, que establece requisitos de calidad y competencia1 Y si este laboratorio desea demostrar que es competente y capaz de emitir resultados válidos y confiables debe optar por una acreditación nacional o internacional con esta norma.
La acreditación es un proceso voluntario, en Latinoamérica, mediante el cual una organización externa declara formalmente que un laboratorio (de ensayos, calibración y clínico), un organismo de certificación (de productos, sistemas y personas) o un organismo de inspección es competente técnicamente para ejecutar actividades específicas. Estos organismos y laboratorios se denominan Organismos de Evaluación de la Conformidad (OEC) y son previamente auditados según una norma ISO específica (Tabla 1).
Tabla 1. Normas a acreditar según laboratorio u organismos
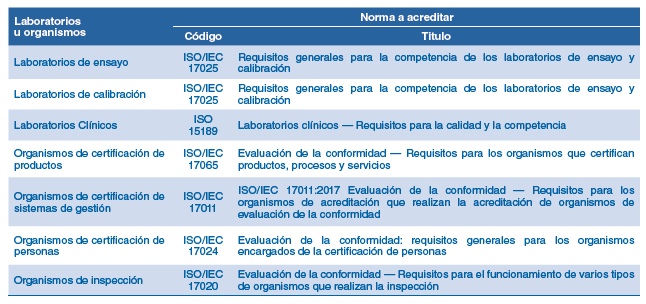
Fuente: Elaboración propia
Cada país cuenta con una o más organizaciones con la autoridad para acreditar los OEC. En el Perú es el Instituto Nacional de Calidad (INACAL)2. Estos organismos deben operar según la norma ISO/IEC 17011 Evaluación de la conformidad — Requisitos para los organismos de acreditación que acreditan a los organismos de evaluación de la conformidad.
Esto organismos de acreditación se agrupan en organizaciones a nivel mundial, por temas y por regiones, previa evaluación por pares, reconocen su competencia para acreditar OEC en determinada norma. Entre ellas el Foro Internacional de Acreditación (IAF)3, la Cooperación Internacional de Acreditación de Laboratorios (ILAC)4 y en nuestra región la Cooperación Interamericana de Acreditación (IAAC)5 (Tabla 2).
Tabla 2. Principales agrupaciones internacionales de organismos de acreditaciones

Fuente: Elaboración propia
Ser miembro implica Acuerdos de Reconocimiento Multilateral (MLA) o Acuerdo de Reconocimiento Mutuo (MRA), en donde las acreditaciones realizadas por cada miembro son reconocidas en los países de todos los miembros.
El INACAL tiene acuerdos MLA y MRA con el IAF, la ILAC y la IAAC, para las normas ISO/IEC 17025, ISO/IEC 17020, ISO/IEC 17065, ISO/IEC 17021-1, ISO/IEC 17021-2, ISO/IEC 17021-3, ISO/IEC 17021-9 y ISO/IEC 17021-10.
Metodología
Para obtener los datos sobre los laboratorios acreditados con la ISO 15189 en Latinoamérica se revisaron las páginas web del Foro Internacional de Acreditación (IAF)3, Cooperación Internacional de Acreditación de Laboratorios (ILAC)4, Cooperación Interamericana de Acreditación (IAAC)5 y la de los organismos de acreditación de cada país latinoamericano.
Se tomo como referencias las publicaciones de Alba C. Garzón6 y Carboni-Huerta Roberto7.
Resultados
En Latinoamérica el número de laboratorios acreditados con la ISO 15189, es muy inferior al número de laboratorios de ensayo o calibración acreditados con la ISO/IEC 17025, en todos los países de la región (Tabla 3).
Es conveniente precisar que los laboratorios clínicos acreditados con la ISO 15189 en cada país, no necesariamente son de ese país. En el caso de Perú, por lo menos dos (02) laboratorios clínicos están acreditados con EMA de México y uno (01) con ENAC de España. Lo mismo ocurre con la ISO/IEC 17025 para laboratorios de ensayos, varios laboratorios están solo acreditados con ANAB de Estados Unidos.
En los organismos de acreditación latinoamericanos las disciplinas/campos de análisis/áreas son similares, solo EMA de México, acredita independientemente disciplinas para los laboratorios clínicos y para los laboratorios de Banco de Sangre. En los demás países “Banco de sangre” es una disciplina/campo de análisis/área. En el Salvador se incluyen todos los procedimientos analíticos como “Análisis clínicos”.
Entre las disciplinas/campos de análisis/áreas más comunes están: química clínica, hematología, microbiología, serología, uroanálisis, inmunología y biología molecular.
Discusión
Si comparamos el porcentaje de laboratorios por país la situación es más preocupante. En Perú el número de laboratorios clínicos según RENIPRES (Registro Nacional de Instituciones Prestadoras de Servicios de Salud) es aproximadamente 5000, entre públicos y privados, y aproximadamente diez (10) laboratorios clínicos acreditados (INACAL, EMA, ENAC) es decir sólo un 0,2 %. En el caso de México el número de laboratorios médicos y de diagnóstico es de 15,152 y son 177 los acreditados, es decir 1,2%. En el caso de Jamaica de sus 52 laboratorio, 15 cuentan con acreditación. Este porcentaje de laboratorios acreditados representa una cifra mayor, 28.9% en comparación con los países mencionados cuyas poblaciones son mayores.
Para el caso de México su población al 2020 es de 126,014,024; en el caso de Perú según el Instituto Nacional de estadística e Informática (INEI) para ese mismo año es de 32,625,948 personas (seleccionar año 2020/Población Estimada y Proyectada/ Población total y descargar el archivo en Excel); y la población de Jamaica al 2020 de sólo 2,881,000.
Tabla 3: Laboratorios acreditados según organismos de acreditación de cada país a junio del 2023
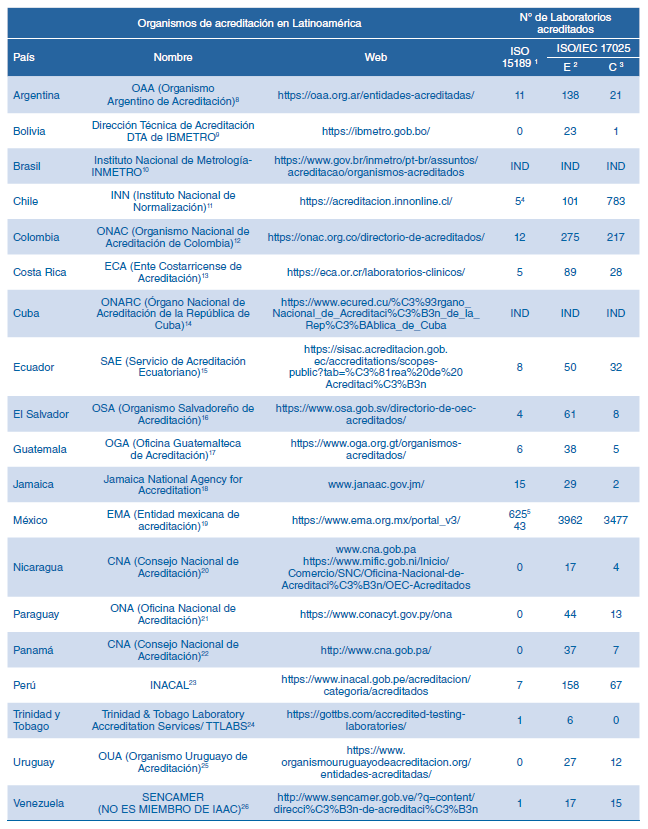
*IND: Información no disponible en la dirección web registrada en IAAC.
1: Se contabilizaron por laboratorio clínico acreditado por sede. En el caso de ensayos y calibraciones no se hizo el filtro. En países como Chile y México un mismo laboratorio tiene varias acreditaciones por sector, disciplina, ramas, magnitud o área.
2: E = Laboratorios de Ensayos
3: C = Laboratorios de Calibración
4: 5 acreditaciones de laboratorios clínicos. De las cuales 04 corresponden al mismo laboratorio, por cada área acreditada.
5: 625 acreditaciones de laboratorios clínicos y 43 bancos de sangre. Si se consideran por laboratorio serian 177 acreditaciones, cada uno en diferentes disciplinas.
Fuente: Elaboración propia
En resumen, el porcentaje de laboratorios clínicos acreditados en Latinoamérica, aquellos capaces de respaldar con resultados válidos y confiables, es muy bajo a excepción de Jamaica. Esta situación es preocupante ya que en la mayoría de los casos el tratamiento de un paciente se basa en gran medida en la confiabilidad de los resultados de laboratorio.
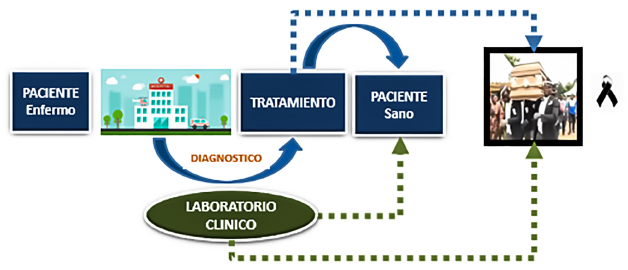
Figura 1: Impacto de los resultados emitidos por un laboratorio clínico en la salud del paciente
Fuente: Elaboración propia
La pregunta podría ser ¿Qué hacer para revertir esta situación? Una alternativa, pero inviable, es establecer que la acreditación de los laboratorios clínicos con la norma ISO 15189 sea obligatoria en Latinoamérica. Este proceso va a requerir acciones a corto y largo plazo. Estrategias como la inclusión de cursos en la malla curricular de los profesionales de salud y técnico de laboratorio clínico sobre gestión de calidad en los laboratorios clínicos, norma ISO 15189. Los que podrían masificarse por parte de las instituciones públicas (por ejemplo, Institutos de Salud, organismos de acreditación, colegios profesionales, universidades). También habría que fortalecer el trabajo en equipos multidisciplinarios en los laboratorios clínicos, sensibilizar a los tomadores de decisión gubernamental, fortalecer la infraestructura de la calidad, priorizar los laboratorios clínicos de los establecimientos de salud de mayor nivel de complejidad, establecer convenios de cooperación entre los organismos de calidad y los Institutos de Salud, universidades, colegios profesionales entre otras instituciones del sector. Finalmente, es fundamental actualizar la normatividad sobre laboratorios clínicos en cada país, alineándolo progresivamente a la ISO 15189.
Joseph Juran, gurú de la calidad: “Los miembros de un EQUIPO VENCEDOR, luchan contra sus competidores, los miembros de un EQUIPO PERDEDOR luchan entre sí”.
Referencias bibliográficas
1. Instituto Nacional de la Calidad. Norma Técnica Peruana NTP-ISO 15189:2023 Laboratorios Clínicos. Requisitos particulares para la calidad y la competencia. 4a ed. Lima: INACAL; 2023. 99 p.
2. Instituto Nacional de Calidad [Internet]. Lima: INACAL; [actualizado 14 de diciembre de 2023]. Disponible en: https://www.gob.pe/inacal
3. International Accreditation Forum [Internet]. Arlingotn, Virginia: International Accreditation Forum; [actualización 8 noviembre 2023]. Disponible en: https://iaf.nu/en/home/
4. International Laboratory Accreditation Cooperation [Internet]. International Laboratory Accreditation Cooperation: Silverwater, Australia: ILAC; 2019. Disponible en: https://ilac.org/.
5. Inter-American Accreditation Cooperation [Internet]. North Carolina: IAAC; [actualización 23 marzo 2023]. Disponible en: https://www.iaac.org.mx/index.php/en/
6. Garzón AC. Sistemas de gestión en el laboratorio clínico en Latinoamérica. EJIFCC [Internet]. 2015;26(4):221-5. Disponible en: https://cms.ifcc.org/media/334081/eJIFCC2015Vol26No4pp221-225.pdf
7. Carboni-Huerta R, Sáenz-Flor K. Acreditación ISO 15189 en América Latina: Percepción en laboratorios de la región. Rev Mex Patol Clin Med Lab [Internet]. 2019;66(3):143-153. Disponible en https://www.medigraphic.com/cgi-bin/new/resumen.cgi?IDARTICULO=89585
8. Organismo Argentino de Acreditación [Internet]. Buenos Aires: OAA; [actualización 15 abril 2020]. Disponible en: https://oaa.org.ar/
9. Instituto Boliviano de Metrología [Internet]. La Paz: Instituto Boliviano de Metrología; [actualización 18 octubre 2023]. Disponible en: https://ibmetro.gob.bo/
10. Instituto Nacional de Metrologia, Qualidade e Tecnologia [Internet]. Rio de Janeiro: INMETRO; [actualizado 14 diciembre 2023]. Disponible en: https://www.gov.br/inmetro/pt-br
11. Instituto Nacional de Normalización [Internet]. Santiago de Chile; Instituto Nacional de Normalización: [actualización 17 diciembre 2023]. Disponible en: https://www.inn.cl/
12. Organismo Nacional de Acreditación de Colombia [Internet]. Bogotá D.C.: ONAC; [actualización 13 octubre 2023]. Disponible en: https://onac.org.co/
13. Ente Costarricense de Acreditación [Internet]. San José: Ente Costarricense de Acreditación; [actualización]. Disponible en: https://eca.or.cr/
14. EcuRed [Internet]. La Habana: EcuRed; [actualización 27 agosto 2009]. Órgano Nacional de Acreditación de la República de Cuba [Internet]. Disponible en: https://www.ecured.cu/%C3%93rgano_Nacional_de_Acreditaci%C3%B3n_de_la_Rep%C3%BAblica_de_Cuba
15. Servicio de Acreditación Ecuatoriano [Internet]. Quito: Servicio de Acreditación Ecuatoriano; [26 noviembre 2016]. Disponible en: https://www.acreditacion.gob.ec/
16. Organismo Salvadoreño de Acreditación [Internet]. San Salvador: OSA; [actualización 5 setiembre 2021]. Disponible en: https://www.osa.gob.sv/
17. Oficina Guatemalteca de Acreditación [Internet]. Ciudad de Guatemala: OGA; [actualización 28 junio 2014]. Disponible en: https://www.oga.org.gt/
18. Jamaica National Agency for Accreditation [Internet]. Kingston: JANAAC; [actualización 9 julio 2022]. Disponible en: https://www.janaac.gov.jm/
19. Entidad Mexicana de Acreditación [Internet]. Ciudad de México: EMA; [actualización 21 junio 2016]. Disponible en: https://www.ema.org.mx/portal_v3/
20. Organismo Nacional de Acreditación [Internet]. Asunción: Organismo Nacional de Acreditación; [actualización 9 abril 2014]. Disponible en: https://www.conacyt.gov.py/ona
21. Consejo Nacional de Acreditación [Internet]. Panamá: Consejo Nacional de Acreditación; [actualización 22 setiembre 2023]. Disponible en: http://www.cna.gob.pa/
22. Gob.pe [Internet]. Lima: Gob.pe; [actualización 27 diciembre 2023]. Instituto Nacional de Calidad; [actualización 15 diciembre 2023]. [aproximadamente 6 pantallas]. Disponible en: https://www.gob.pe/inacal/
23. Trinidad & Tobago Bureau of Standards [Internet]. Tunapuna: Trinidad & Tobago Bureau of Standards; [actualización 24 noviembre 2018]. Trinidad & Tobago Laboratory Accreditation Services; [actualización 6 octubre 2012]. [aproximadamente 4 pantallas]. Disponible en: https://gottbs.com/ttlabs/
24. Organismo Uruguayo de Acreditación [Internet]. Montevideo: OUA; [actualización 18 agosto 2023]. Disponible en: https://www.organismouruguayodeacreditacion.org/
25. Servicio Desconcentrado de Normalización, Calidad, Metrología y Reglamentos Técnicos [Internet]. Caracas: SENCAMER; [actualización 30 agosto 2023]. Disponible en: https://www.sencamer.gob.ve/










